Ангиогенеза се нарича процесът на формиране на нови кръвоносни съдове - първично, по време на ембрионалното развитие на човека, а също и вторично, при травми на всички видове тъкани в организма с последващата им регенерация. Сърдечно - съдовата система представлява се диференцира първа (като самостоятелна система) по време на ембриогенезата на всички гръбначни животни - до момента на нейното обособяване се наблюдава единствено делене на клетките без никакви признаци на диференциация. Освен това системата е първата, която започва да функционира - което е логично, тъй като доставя всички необходими хранителни вещества и кислород, необходими за растежа и развитието на организма. Тъй като ангиогенезата е от ключово значение освен това и за оздравителните процеси, тя ще бъде разгледана в детайли в тази секция на нашия сайт. Всеки дентален лекар, който поставя зъбни импланти, е необходимо да познава в детайли оздравителните процеси в човешкия организъм - както при костите, така и в пределите на меките тъкани. Ангиогенезата има решаващо значение при тях - без прорастване на нови съдове в дадена област не е възможно да се образува нито нова костна тъкан, нито съединителна тъкан и епител. Без прорастване на нови кръвоносни съдове не е възможно да оздравее и вече наличната нормална тъкан, която във всеки един случай е увредена от оперативната интервенция. Все пак, при единичен разрез в областта на здравата лигавица и периост прорастването на нови капиляри има много по-малко клинично значение, отколкото при костната пластика в по-голям обем например. Колкото е по-голям обемът на новите тъкани, които е необходимо да се образуват, толкова по-решаващо значение има ангиогенезата за безпроблемното протичане на оздравителните процеси. Поради всички тези закономерности нашият екип смята за небходимо да отдели внимание на този крайно интересен биологичен процес - формирането на нови кръвоносни съдове. Всъщност това формиране се случва през целия живот на човека - от момента на образуване на първите кръвоносни съдове вътреутробно до дълбока старост; най-общият принцип е че при промяна в метаболитната активност на всяка една тъкан е налице и промяна в нейната степен на васкуларизация. При атрофия на тъканите силно намалява и количеството на кръвоносните съдове в тях за единица обем; обратно, при хипетрофия нараства и броят, и калибърът на наличните артерии, капиляри и вени. В някои случаи намаляването на количеството кръвоносни съдове може да бъде следствие от атрофията на тъканите (например при афункционалната атрофия), а в други - причина за нея - например при различни периферни капиларопатии, които влошават изхранването на тъканите и като следствие те намаляват своя обем. При мастната тъкан нарастването на теглото на целия организъм води до увеличаване на количеството на кръвоносните съдове, докато отслабването води до намаляването им. Същите принципи са валидни и при телесната мускулатура - интензивните тренировки водят до образуването на повече съдове с по-голяма калибър, а липсата на функционална активност намалява количеството им. Поради това спортистите имат силно изразени, изпъкнали вени - особено в областта на предмишницата, което силно улеснява вземането на кръв. От клинична гледна точка всичко това е от голямо значение за областта на микросъдовата хирургия - при нея хиперстеничният хабитус е силно благоприятен фактор, докато за повечето други области на хирургията подобно телосложение може да доведе единствено до затруднения по време на оперативната интервенция.
Шотландският анатом Джон Хънтър за първи път се опитва да опише ангиогенезата - което се случва през 1794 година. Той все пак не въвежда термина ангиогенеза, но забелязва положителната корелация между метаболитната активност на дадена тъкан и нейното кръвоснабдяване. В своите трудове Джон Хънтър се базира на едно схващане, формулирано още по времето на Аристотел - формата следва функцията. Древногръцкият философ е бил изключително наблюдателен човек и съвсем правилно е забелязал че при активно спортуващи атлети мускулатурата е хипертрофична и добре оформена. В следващите векове други изследователи установяват че същото твърдение е валидно и за кръвоснабдяването. Едва през 1971 година обаче Юда Фолкман изказва хипотезата че също и туморният растеж е възможно да бъде зависим от ангиогенезата - като това твърдение е всъщност доста логично, тъй като при интензивни обменни процеси се изисква доста по-добро кръвоснабдяване. Впоследствие ангиогенезата при неопластичните процеси е проучена изключително детайлно, тъй като е установено че нейното подтискане като цяло е възможно да доведе до регресия на новообразуванието. Установено е също така че първоначално при всеки един тумор (от най-доброкачествения до най-малигнения) има аваскуларна фаза. При нея има едиснтвено група от клетки, които се делят непрекъснато и независимо от регулаторните системи на организма. Впоследствие се преминава към ангиогенетичната фаза - неопластичните клетки формират ангиогенетичен фенотип, който в крайна сметка води до разрастване на нови и нови кръвоносни съдове.
Първите ендотелни клетки се генерират след гаструлацията - усилено делене и растеж на клетките, които се подреждат в зародишни пластове. Това се случва по време на най-раните етапи от развитието на ембриона. Ендотелни клетки се диференцират от клетки, наречени ангиобласти, едновременно с подреждането им в къси кръвоносни съдове. Тези първоначални кръвоносни съдове растат и се свързват помежду си, за да образуват мрежа. По-късно в кръвоносните съдове се включват фибробласти (основни клетки на съединителната тъкан) и мускулни клетки. Първоначалната мрежа от кръвоносни съдове преминава през непрекъснат процес на ремоделиране по време на тези етапи на развитие - а всъщност и през целия живот на човека. При ембриона всички ендотелни клетки са сходни, но прогресивно се диференцират в ендотел на вените, артериите, капилярите и лимфните съдове. Някои гени (FGF2, BMP4, IHH и VEGF) индуцират отделните пътища на диференциация.

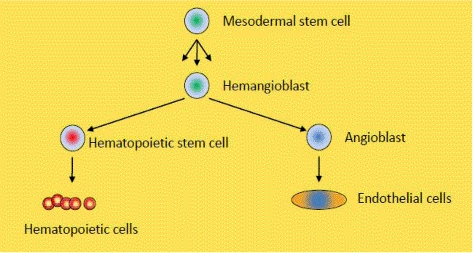
Схема на първоначално формиране на кръвта и кръвоносните съдове. Този процес се осъществява на много ранен етап от вътреутробното развитие на човека - още през първите гестационни седмици поради важността на сърдечно - съдовата система за оцеляването и развитието на целия организъм. От мезодермалните стволови клетки се образуват хемангиобласти; те от своя страна се диференцират в две посоки - хемопоетични стволови клетки и ангиобласти. От първите се образува всяка една кръвна клетка, а вторите дават началото на ендотелните клетки.
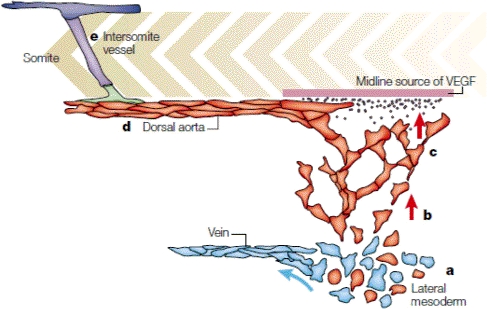
Ембионално развитие на кръвоносните съдове - постепенно ендотелните клетки се подреждат маншонообразно и формират просвета на съда. Това се случва както интраембрионално, така и екстраембрионално - при пъпната връв и плацентата, без които не е възможно да се развива нито един зародиш. Първоначално се образуват съдовете с най-голям калибър - коремната аорта и двете кухи вени. Впоследствие между тях прорастват капиляри - които на горната схема са означени с латинските букви c и b. Постепенно капилярната мрежа се усложнява и обхваща всички органи и тъкани.
Описана е така наречената кълнова ангиогенеза - кръвоносните съдове прорастват буквално както растат клоните на дърветата и растенията изобщо. Хипоксията има мощен стимулиращ ефект върху този тип ангиогенеза - очевидно е че след като в даден участък от тъканите има липса на кислород, то е необходимо в тази посока да прорастнат нови кръвоносни съдове. При липса на кислород и хранителни вещества паренхимите клетки на всяка една тъкан в организма секретират съдовия ендотелен растежен фактор (VEGF-A - Vascular Endotel Grwoth Factor A), който е сигнал за ендотелните клетки за започване на процес на делене. Въпросните еднотелни клетки секретират протеолитични ензими, които лизират базалната мембрана на съда - тя се разрушава и ендотелната клетка излиза извън централния съдов ствол, за да формира съдово клонче. Именно това представлява процесът на разклоняване на съда. Ендотелната клетка, която първа секретира протеолитичния ензим, се нарича върхова клетка (tip cell) и има ключово значение за процеса на ангиогенезата - именно тя първа получава биологичния сигнал за тъканно увреждане, съответно необходимост от формиране на нов кръвоносен съд. След тази клетка мигрират нови и нови ендотелни клетки, наречени стръкови (stalk cells), като постепенно се формира лумен (просвет) на кръвоносния съд. Важно е между пролифериралите ендотелни клетки да се формират плътни междуклетъчни контакти - това става с помощта на структурния протеин интегрин, който осигурява плътната връзка между отделните клетки. От физиологична гледна точка това е важно - при липса на плътен контакт между ендотелните клетки системата на кръвосъсирването получава сигнал за увреждане на кръвоносния съд и бързо се активира, за да предотврати потенциалния кръвозлив. Това активиране обаче може да доведе и до негативни последици - тромбозиране на кръвоносни съдове и влошаване на изхранването на тъканите. Именно това представлява патогенезата на всеки един инфаркт - запушване на кръвоносен съд в дадена област на организма с всички негативни последици от това. Инфарктите на жизненоважни тъкани и органи са основна причина за смъртността при хората в в световен мащаб - всъщност дори са на първо място като етиологичен фактор и едва на второ са неопластичните процеси. Поради това тромбозирането и фибринолизата са изучени изключително подробно през последните няколко десетилетия - профилактиката на образуването на съсирек може да спаси живота на всеки един пациент, а лизирането на един вече сформиран тромб може да съхрани виталитета на всяка една жива тъкан.
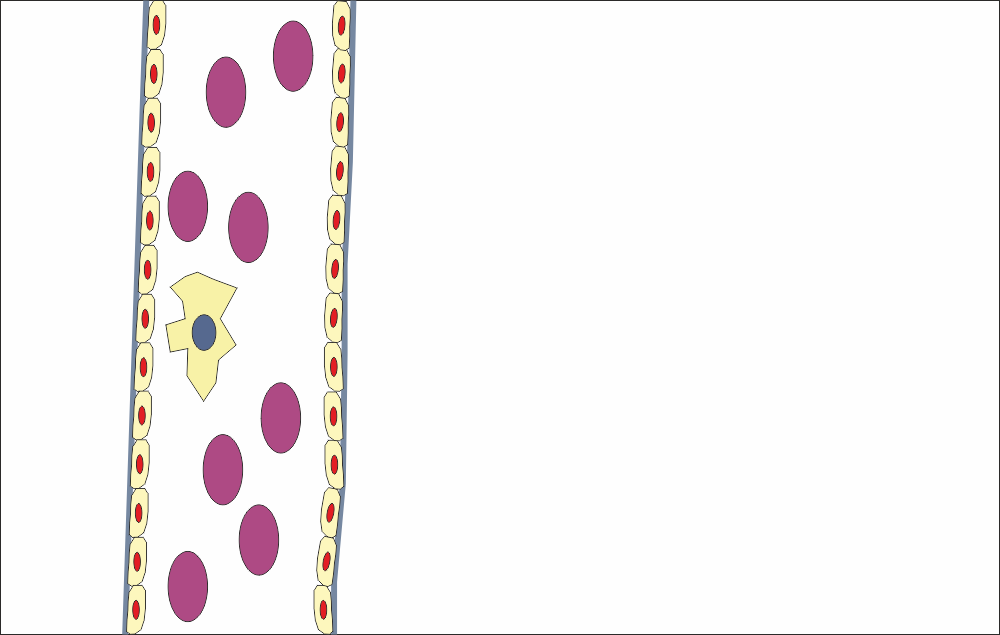
Първоначална ситуация - нормален кръвоносен съд, изпълнен с кръвна плазма и формени елементи. Виждат се няколко еритроцита и единичен левкоцит. В съседните тъкани липсва увреждане, ситуацията изглежда нормална - доколкото нещо в човешкия организъм изобщо може да бъде нормално. Базалната мембрана на кръвосносния съд е запазена, покрита е с един слой ендотелни клетки. При нормлани условия ендотелът представлява еднослоен плосък епител, изключително рядко - еднослоен кубичен епител. Това всъщност е единственият еднослоен плосък епител в организма - няма необходимост от по-сериозна механична бариера, а единствено от тъкан с изолираща функция. Същевременно точно този епител, на пръв поглед елементарно устроен, играе огромна роля в цялата човешка патология. Немалка е ролята на ендотела и при физиологични условия - и тъй като физиологичните и патологичните процеси в човешкия организъм много често са изключително тясно преплетени и протичат в много тясна взаимовръзка, изучаването им в детайли е от огромна полза за всеки един теоритик или практикуващ лекар в която и да е област на медицината.
При възрастни лица скоростта на пролиферация на ендотелните клетки е много ниска. Например ендотелната клетка може да се дели веднъж месечно или дори на няколко години. Ангиогенезата протича рядко във всички видове тъкани при нормални физиологични условия - с изключение на женските репродуктивни органи. По време на месечния цикъл маточната обвивка (ендометриум) се обновява изцяло, тъй като се подготвя за евентуален процес на оплождане - имплантиране на ембриона в маточната стена. Въпреки тази забавена обмяна ендотелните клетки е възможно да се активират при патологични процеси като тъканни увреждания и тумори. Някои вещества индуцират ангиогенеза, като ендотелен растежен фактор (EGF), фибробластен растежен фактор (FGF), трансформиращ растежен фактор (TGF) и простагландини. Ангиогенезата започва когато ангиогенни вещества се отделят от околните тъкани. Обикновено ендотелните клетки показват силно намален метаболизъм, като последният е основно под формата на гликолиза - анаеробно разграждане на глюкозата, при което се генерира енергия. Гликолизата в случая има голям биологичен смисъл - тя е потенциален източник на енергия, тъй като новите кръвоносни съдове могат да възникнат в области с ниско съдържание на кислород. Ендотелна клетка на близките кръвоносни съдове, обикновено във венула, която е изложена на най-високата концентрация на сигнали, започва да мигрира към източника на ангиогени сигнали, увличайки другите ендотелни клетки, които започват да се размножават и образуват нов кръвоносен съд. Когато ендотелните клетки не получават правилни сигнали, те умират чрез апоптоза (програмирана клетъчна смърт) или се превръщат в мезенхимни клетки, които могат да синтезират обилен извънклетъчен матрикс. Преходът от ендотелна към мезенхимна клетка е свързан с някои заболявания като атеросклероза и фиброзен миокардит.
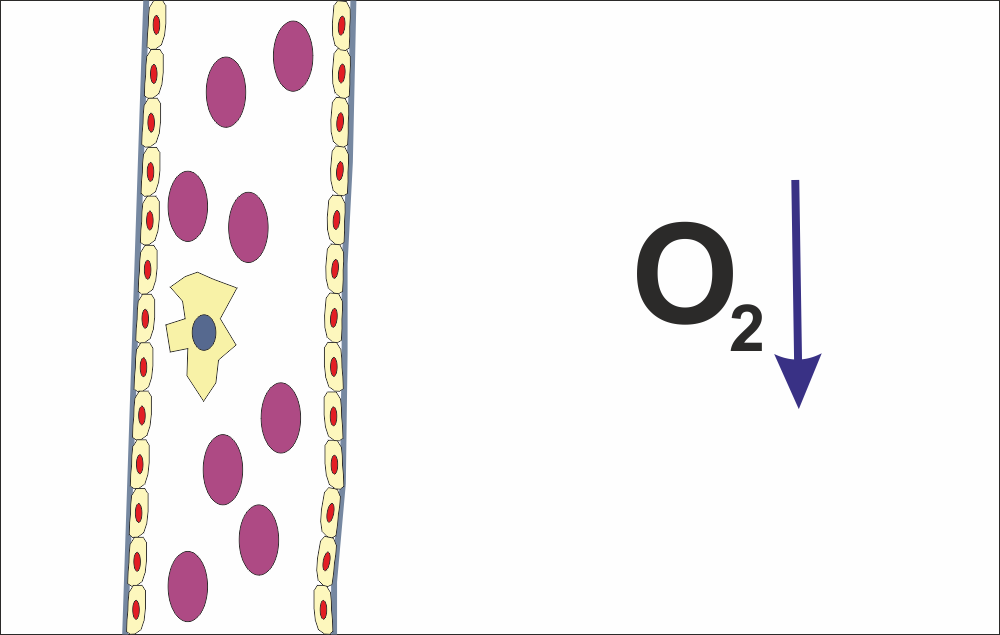
Хипоксията представлява намалено съдържание на кислород в тъканите. Това е важен биологичен сигнал за ангиогенезата - показва потенциално тъканно увреждане, тъй като няма друга причина за намалено съдържание на кислород в тъканите. Нещо не е наред и следва да се задейства процес на регенерация - в хода на еволюцията се е разработил именно такъв сигнален механизъм. Нещо подобно се случва и при оперативните интервенции с цел изграждане на костен обем - костна пластика. В този случай човекът просто използва биологичните механизми на регенерация с лечебна цел - или, както е казал още Хипократ, медицината единствено се стреми да наподобява лечебните способности на природата. При костната пластика има една съществена разлика - като изключим атрофията, подлежащият на костна аугментация участък е клинично здрав, патологични изменения в него просто липсват. Атрофията е почти изцяло физиологичен процес. В други случаи ситуацията е коренно различна - ниското съдържание на кислород в даден тъканен участък най-често е резултат от некроза, която има различна етиология и патогенеза, но във всички случаи е необходимо да се възстанови. По възможност възстановяването трябва да бъде пълно - restitutio ad integrum, което в много случаи е възможно, а в други е съпроводено с тъканни изменения.
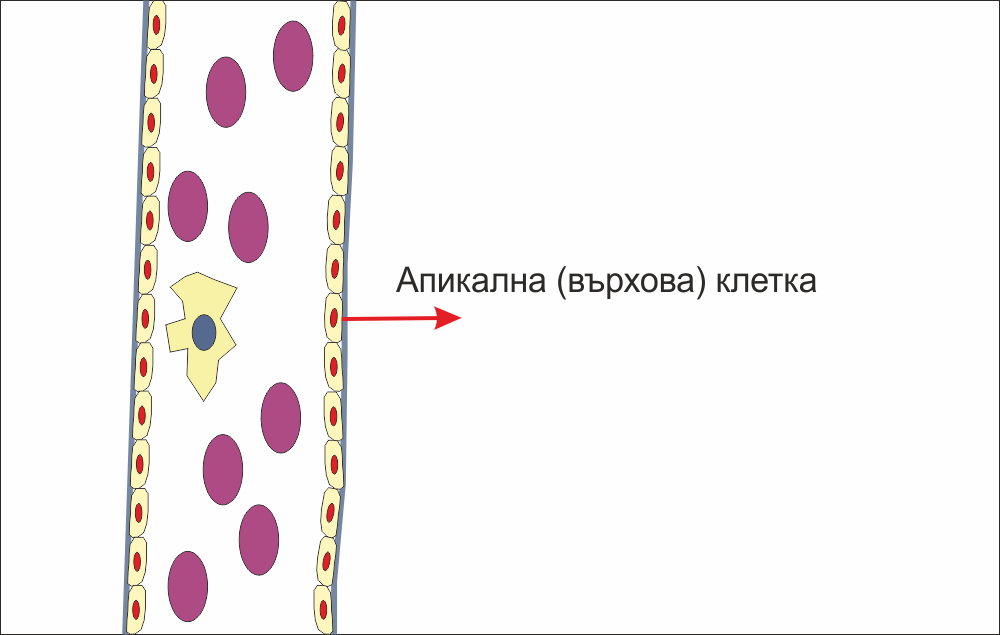
Биологичният (биохимичен) сигнал за тъканно увреждане е получен и е необходимо организмът да предприеме нещо. При липса на адекватни мерки от страна на тялото потенциалните последици няма да са особено благоприятни, така че еволюцията се е погрижила за това - тъканите трябва да се възстановят. Една клетка реагира първа, като секретира протеолитични ензими и лизира базалната мембрана. Към настоящия момент не е известно по какъв точно начин въпросната клетка усеща хипоксията в съседство с кръвоносния съд - физиолозите и патофизиолозите е необходимо да си блъскат главите върху това, а ние като клиницисти просто ще се възползваме в ежедневната си клинична работа от този механизъм на регенерация. Ендотелната клетка, която реагира първа, се нарича апикална клетка - нищо общо с апекса на зъбния корен, който е основна цел в съвременната ендодонтия.
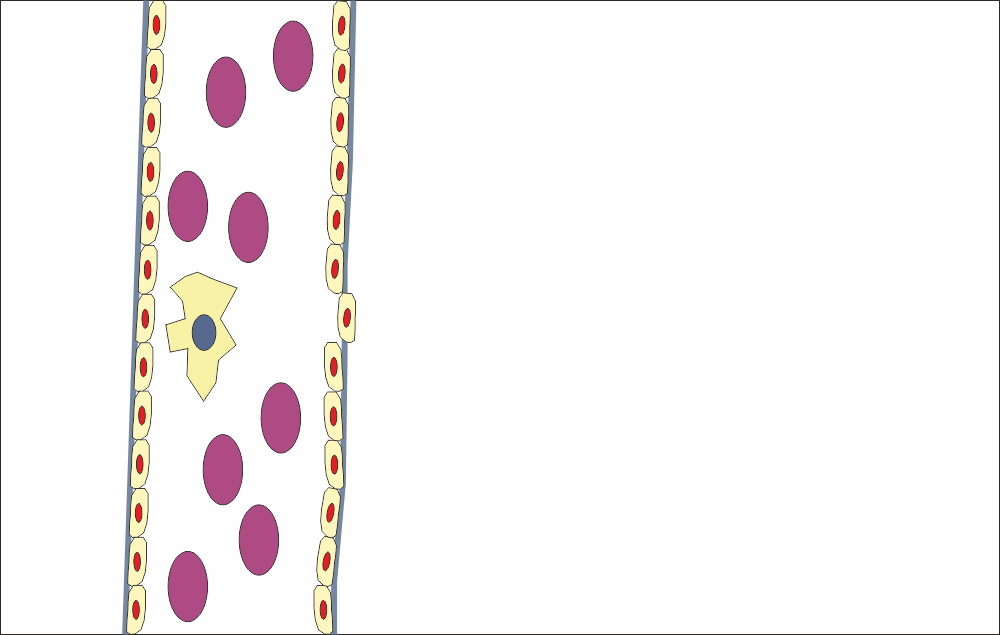
Миграция на апикалната клетка в посока базалната мембрана. Тъй като въпросната мембрана е изградена от плътен колаген и е механично устойчива, нейното разрушаване изобщо не е толкова лесно. За тази цел апикалната клетка отделя протеолитични ензими. След деструкцията на мембраната ендотелната клетка мигрира в пределите на исхемизираните тъкани и дава началото на новия кръвоносен съд.
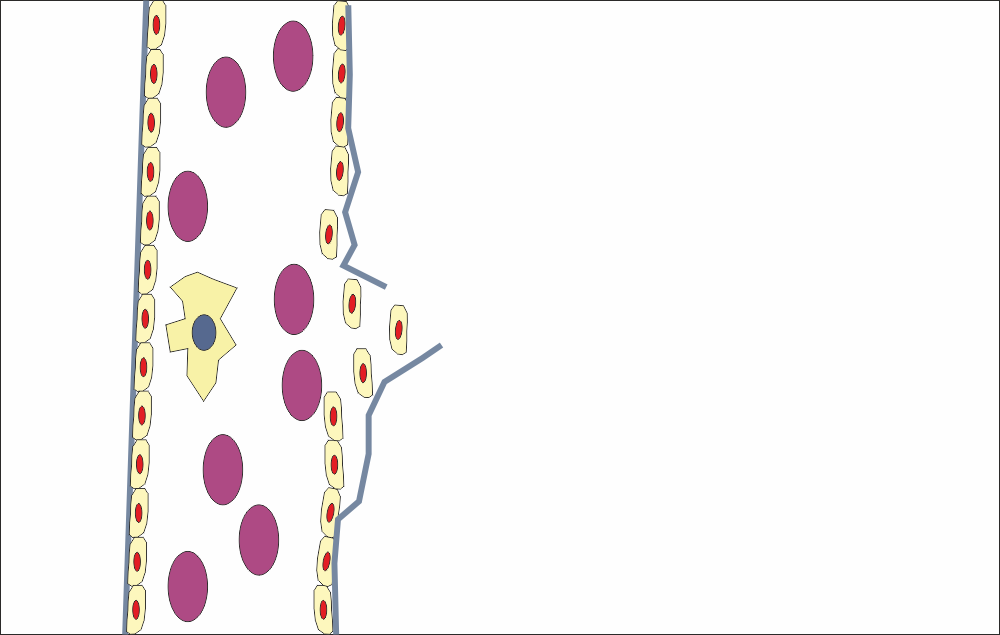
Постепенно и съседните ендотелни клетки започват да мигрират към участъка, който подлежи на регенерация. Едновременно с това стартира и пролиферация (размножаване) на клетките - тъй като от чисто геометрична гледна точка не е възможно същият брой клетки да покрие по-голяма площ. С нарастването на кръвоносния съд е необходимо да се покрива все по-голяма площ, така че са необходими и все повече нови ендотелни клетки. Успоредно с това се увеличава и площта на базалната мембрана - която се състои основно от колаген, секретиран от околната съединителна тъкан. Именно тя се видоизменя и дава началото на tunica media - гладкомускулният слой на артериите, на базалната мембрана и на околосъдови опорни съединителнотъканни елементи. При капилярите такъв мускулен слой липсва, като той е наличен в минимална дебелина и при вените - предимно отделни мускулни влакна, и то основно при млади идивиди.
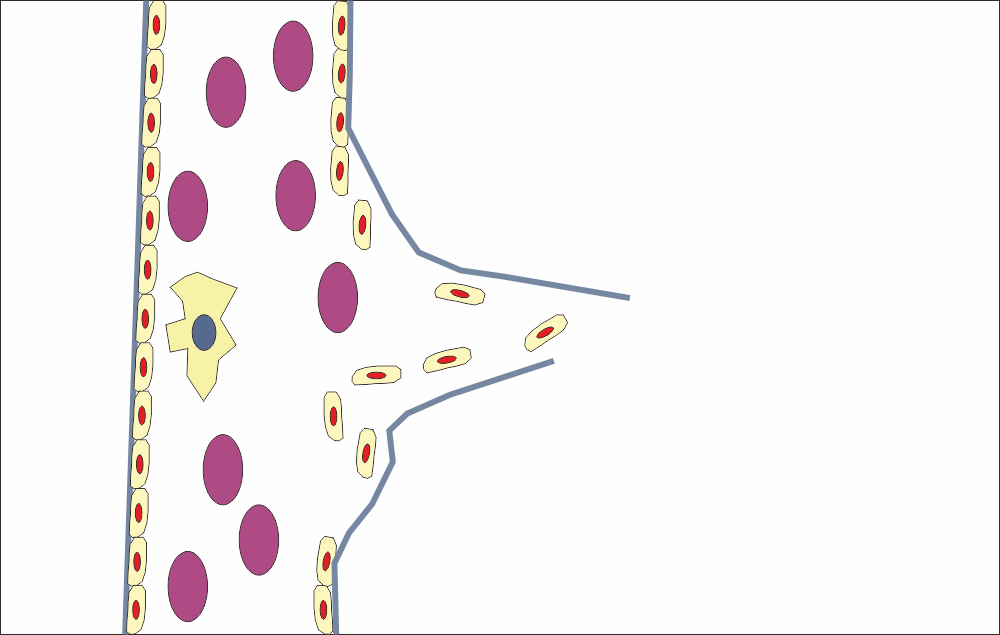
Постепенно базалната мембрана оформя цилиндричен израстък, който дава началото на новия капиляр. Мембраната се състои от плътен колаген - както вече стана въпрос, той се синтезира от фибробласти, които са налични във всяка една тъкан в човешкия организъм. Ендотелните клетки мигрират в посока новосформирания цилиндър и постепенно покриват новосинтезираната базална мембрана. Всички тези процеси се регулират прецизно от медиаторите на организма - белтъчни молекули, които активират или подтискат клетъчната пролиферация.
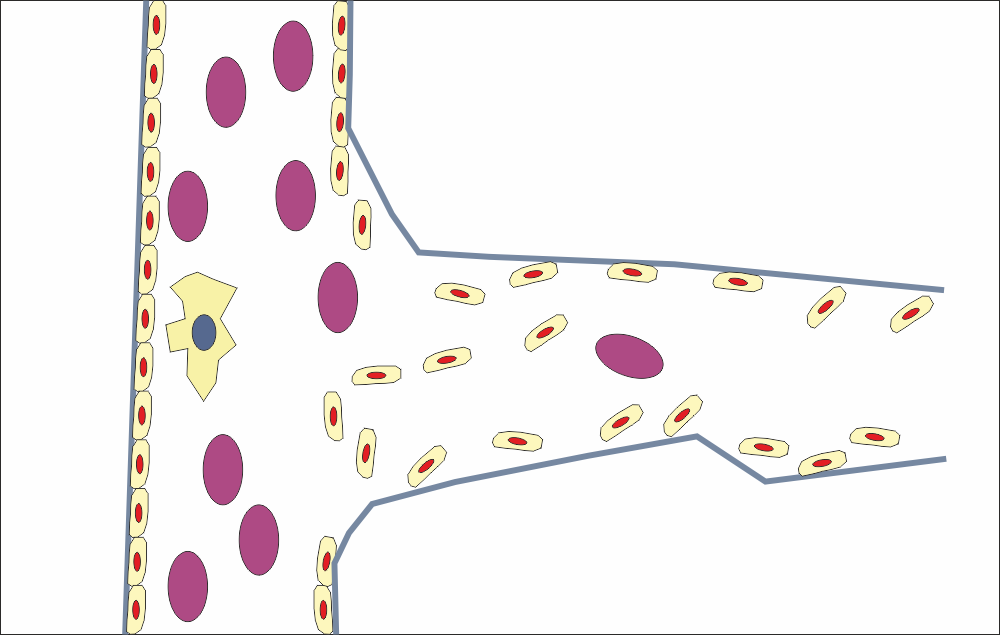
Постепенно новосформираният кръвоносен съд прораства в дълбочина. Пролифериращите ендотелни клетки се подреждат все повече по базалната мембрана, а в лумена (просвета) на съда навлизат формени елементи. С елипсовидна форма с цвят магента са означени еритроцитите, а с многоъгълна форма с налично ядро - левкоцитите. Това се случва още преди да има напълно оформен нов кръвоносен съд, тъй като хипоксичната зона представлява сигнал и за всички формени елементи на кръвта - те се насочват там, за да доставят кислород и необходимите хранителни вещества (еритроцитите и плазмата) или да елиминират потенциални налични инфекциозни агенти (левкоцитите). Част от тези формени елементи, а също и кръвна плазма, излизат извън кръвоносните съдове - поради което и в зоните на хипоксия се наблюдава оток, има хиперемия и еритем, а понякога дори и промяна в цвета на тъканите без да има предварителна механична травма. При механични удари (размачкване на тъканите, удар с тъп предмети) някои малки кръвоносни съдове се разкъсват и плазмата и кръвните клетки неминуемо се изливат в междуклетъчните пространства. Дори и без механична травма обаче в процеса на ангиогенезата има отворени кръвоносни съдове - т.е. кръвоносната система на човека се превръща от такава от затворен тип в такава в отворен, каквато има при по-нисшите животни. По време на ембионалното развитие на организма сърдечно - съдовата система за много дълъг период, до нейното пълно анатомично формиране, е отворена - кръвта не се движи само в кръвоносните съдове, а изтича в различни телесни кухини и междутъканни пространства. Според биолозите онтогенезата е кратко повторение на филогенезата - всеки един жив организъм се развива по начин, който донякъде повтаря еволюцията на биологичния вид. Оказва се обаче че при заздравителния процес на рани също се наблюдават части от механизма на филогенезата - за кратко време кръвоносната система е от отворен тип.
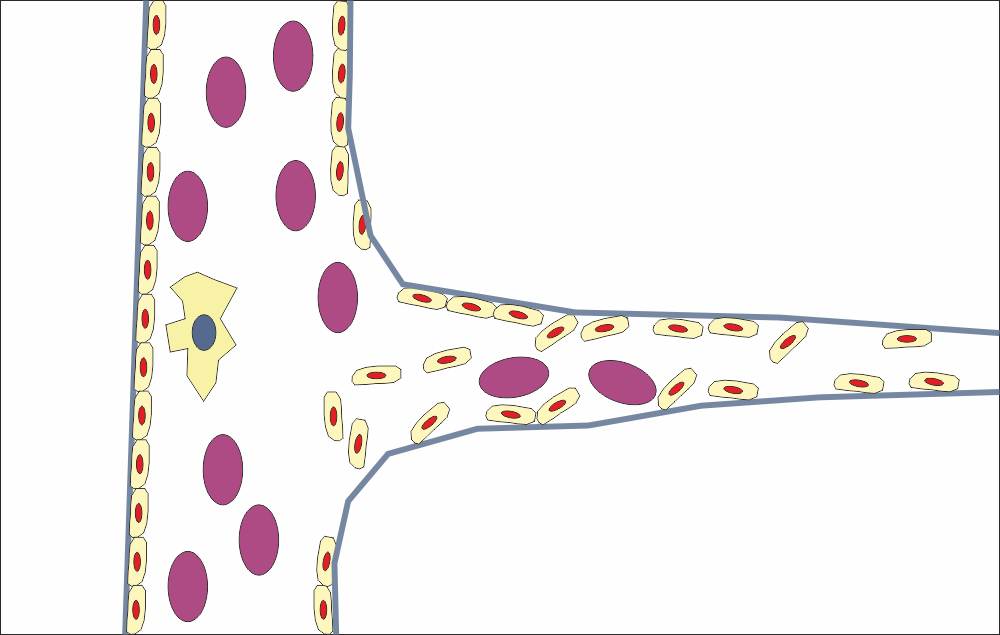
В някои случаи процесът не протича съвсем безпроблемно - вижда се как една ендотелна клетка застъпва базалната мембрана на мястото на разклоняване на новия капиляр. Това не се дължи на мързел или немарливост от страна на графичния дизайнер - направено е с умисъл и цел. Дори и природата не е създала съвършени механизми за възстановяване на живите организми, та какво остава за хората? В нито една човешка дейност няма гарантиран резултат; такъв има при природните закони, но дори и там винаги има известна условност.
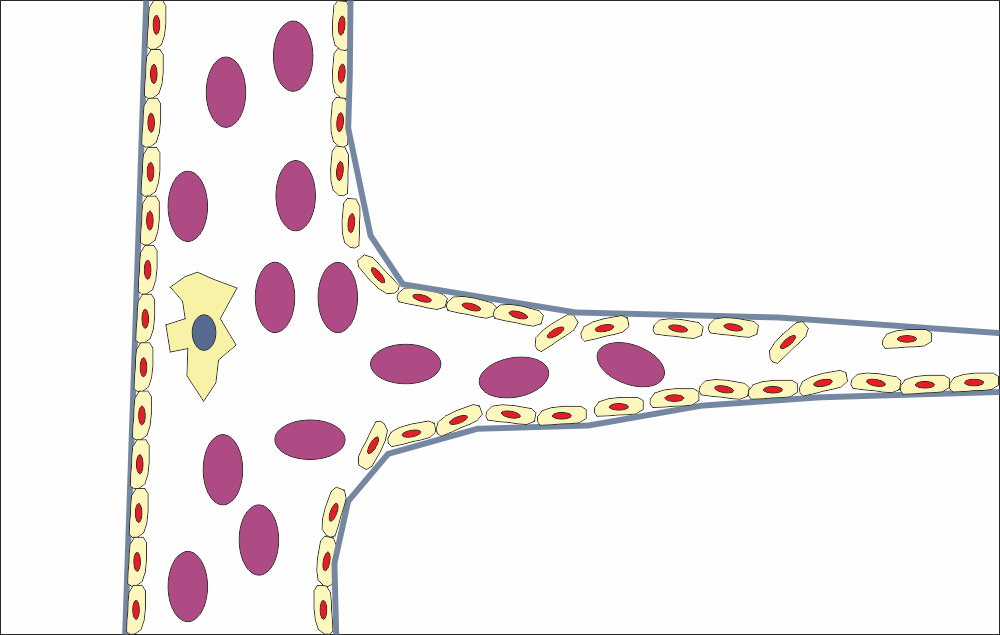
Графична схема на оформянето на нови капиляри. Във фазата на интензивен растеж на гранулационната тъкан всъщност се образуват много повече кръвоносни съдове, отколкото е необходимо за нормалното кръвоснабдяване на тъканите и органите. В даден момент една значителна част от новите капиляри претърпява обратно развитие - регрес. Описани са множество белтъчни молекули, които регулират и този процес - това са така наречените антиангиогенни фактори, които са антагонисти на ангиогенните фактори. Всички процеси на растеж и обратно развитие в живите организми всъщност протичат успоредно; в началото на заздравяването на раните преобладава растежът, а в по-късните фази - обратното развитие (атрофия или апоптоза). При това обратно развитие се получава един вид узряване на новосформираните тъкани - те вече не са толкова интензивно кръвоснабдени, а метаболизмът и размножаването на клетките в тях донякъде се забавя. Всичко това изисква прецизна регулация, при нарушаването на която се стига до развитието на тежка патология - неопластични формации, които са с толкова по-агресивно биологично поведение, колкото повече са нарушени процесите на подтискане на растежа. Ендотелът не прави никакво изключение от тази биологична закономерност - при липса на регулации в растежа на клетките се отключва развитието на хемангиоендотелиом, който представлява агресивна малигнена формация. Подтискането на растежа пък води до затруднено заздравяване на раните - то се наблюдава обикновено при захарен диабет тип 2. При това заболяване са налице периферни ангиопатии, които водят до забавени и затруднени оздравителни процеси. Това следва да се има предвид при поставянето на зъбни импланти при диабетици - необходими са постоянни грижи за оперативната рана, предписване на антибиотици в малко по-високи дози и най-вече - корекция на кръвнозахарните нива от ендокринолог. Това е най-добре да се извърши предоперативно, тъй като профилактиката винаги е добре да се провежда първично, а не вторично или третично.
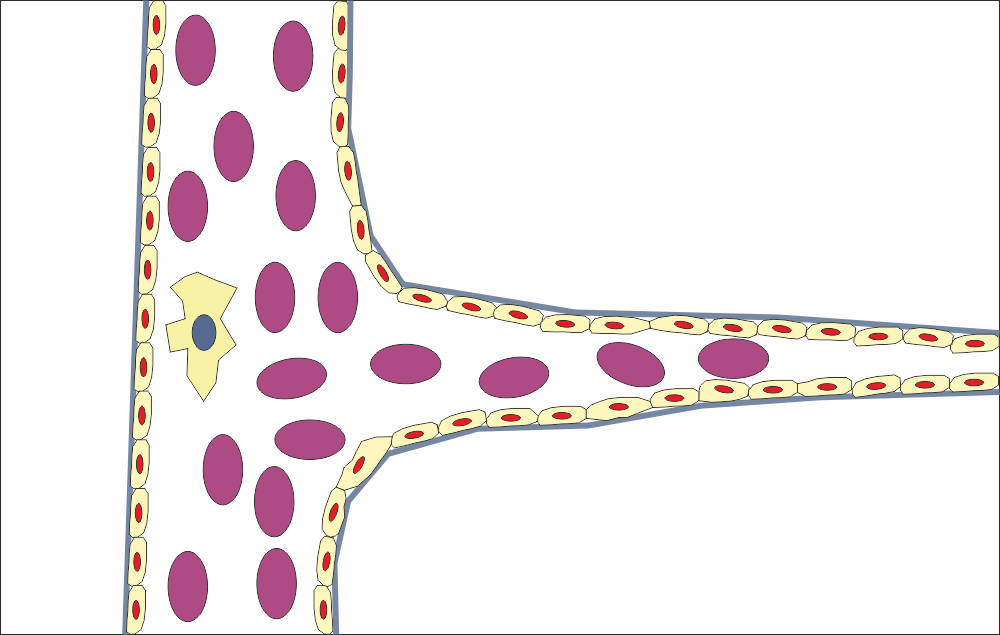
Новият кръвоносен съд е сформиран напълно и започва да изпълнява своята функция. Разбира се, висшите организми като боайниците имат затворено кръвообръщение и нито един кръвоносен съд не завършва на сляпо или в телесна кухина - всеки един прорастващ капиляр или артериола рано или късно се среща с друг, срещулежащ съд, при което се формира анастомоза. Успоредно с този процес във всеки един съд навлизат еритроцити и левкоцити и по този начин започва регенерацията на исхемизираните тъкани - без значение каква е причината за исхемията. Без обилно кръвоснабдяване възстановяването на тъканите става невъзможно и в много клинични ситуации това представлява значителен проблем.
Тъй като една огромна част от тежките патологични процеси в човешкия организъм се дължи именно на запушване на кръвоносни съдове, стимулирането на ангиогенезата като цяло би могло да реши доста тежки здравословни проблеми - както вече стана въпрос. От чисто клинична гледна точка познаването на механизма на тези процеси може да доведе до значително по-успешното лечение на голям брой тежки заболявания. Скоростта на ангиогенезата обаче е несъизмерима със скоростта на формиране на тъканните увреждания - което в случая представлява съществен проблем. Така например при инфаркт на миокарда само след 60 минути настъпва клетъчна смърт - кардиомиоцитите в участъка, засегнат от инфаркта, се увреждат необратимо и на тяхно място разраства съединителна тъкан. Тя обаче не притежава функционалната активност на сърдечната мускулатура - не може да се съкръщава и отпуска, а има единствено опорна функция (съхранява анатомичната цялост на сърцето). При запушване на мозъчни кръвоносни съдове положението е още по-тежко - само след 5 минути настъпва некроза на засегнатия участък от нервната система, което също представлява необратимо увреждане. Към настоящия момент от развитието на медицината не съществува метод, по който да се предизвика прорастване на кръвоносни съдове в рамките на 5 или на 60 минути - процесът отнема няколко дни или дори седмици, за което време тъканите се увреждат необратимо. В обозримо бъдеще едва ли ще бъде въведен метод за толкова бърза регенерация на съдовете - като дори е съмнително дали подобен процес изобщо е възможен. По-вероятно е с помощта на методите на генното инженерство да бъде предизвикано клетъчно делене на неврони или кардиомиоцити; както е известно, тези групи клетки са загубили способността си да се делят още преди раждането на индивида. Ускоряването на процеса на ангиогенеза обаче би могло да бъде от огромна полза при лечението на изгаряния, измръзвания и в пластичната хирургия като цяло. Така например при изгаряне на крайник процесите на некроза се развиват в рамките на няколко дни - в зависимост от обема на изгарянето. При ускоряването на ангиогенезата в бъдеще би могла да бъде избегната ампутацията на засегнати крайници, което също би представлявало един значителен пробив в медицината. Проблем в случая представляват инфекциозните процеси, които се развиват при обширни изгаряния - именно те довеждат до септични състояния с последващата смърт на пациента. Освен това при всяко едно изгаряне е необходима адекватна реанимация, тъй като през изгорената кожна повърхност се осъществява огромна загуба на течности - най-вече поради изпарението им, но също и поради изтичането на кръвна плазма през увредените съдове към външната среда. В областта на реанимацията обаче съвременната медицина има доста повече успехи, отколкото при борбата със септичните състояния.
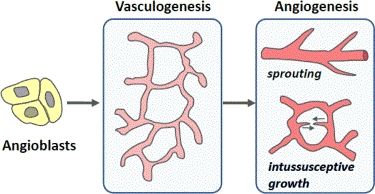
Вляво е показана първичната ангиогенеза, която се осъществява предимно по време на ембрионалното развитие на човешкия организъм. Много по-рядко нещо подобно се случва при зрелите индивиди - при необходимост от зарастване на рани, формиране на нови тъкани при налични дефекти, костна пластика и други обстоятелства. Ангиобластите формират мрежа от кръвоносни съдове. При възрастни индивиди много по-често се наблюдава вторичната ангиогенеза - наличните кръвоносни съдове се разклоняват като растителни кълнове или срещуположни съдове се съединяват като тръба на телескоп - извършва се нещо, подобно на инвагинация. Английският термин intussusceptive има подобно значение, въпреки че се използва и при интестиналната обструкция в коремната хирургия. При ембрионите също понякога се наблюдава подобна ангиогенеза - тъй като растежът е изключително бурен, а хранителните ресурси са ограничени. В българския език не съществува термин, който да възпроизвежда точно значението на наглийската дума intussusceptive - вероятно най-близкото значение има думата разклонителен. Инвагинация означава вгъване, прегъване, но значението на този специфичен термин не се припокрива с думата intussusceptive. Удължаването на един телескоп може би описва визуално най-точно значението на термина; тъй като функцията на езика е да предава информация, българският език определено търпи провал в тази ситуация.
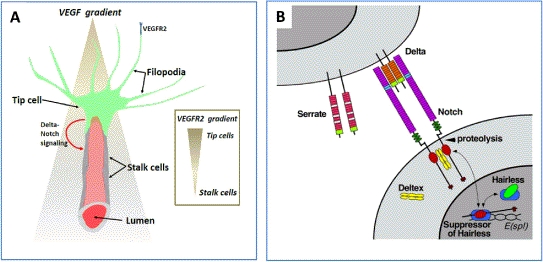
Микроанатомия и микрофизиология на прорастването на нови капиляри - така наречените съдови стволчета или кълнове. Понякога незрелите кръвоносни съдове се наричат още филоподи - означени на горната схема като свежозелени клонки. С повишаването на концентрацията на съдовия ендотелен растежен фактор (VEGF - vascular endothelial growth factor) започва миграцията на клетки - първоначално мигрира апикалната клетка, а след нея - кълновите клетки. Вторият тип клетки следва апикалната клетка и така капилярното клонче постепенно се удължава. Развиват се вакуоли (мехурчета), които постепенно се сливат и се образува съдов лумен - както вече беше показано по-горе. При среща на две апикални (върхови) клетки бързо се формира капиляр от затворен тип, който е основният тип кръвоносен съд при повечето бозайници - те имат така нареченото затворено кръвообръщение, което означава че кръвта като цяло не напуска артериите, вените и капилярите и не тече свободно в телесните кухини. След формирането на затворен капиляр в него бързо започва да тече оксигенирана кръв - с което основният етап от ангиогенезата приключва. Когато тъканите започнат да получават адекватно количество кръв, наситена с кислород, концентрацията на ендотелния растежен фактор рязко намалява. На втората част от фигурата (схема В) е показан интерстициалният градиент на съдовия ендотелен растежен фактор - при повишаването му започва отделянето на протеолитични ензими от апикалната клетка, след което се лизира базалната мембрана и започва прорастване на кръвоносен съд. Ендотелни клетки, които са изложени на максимална концентрация на въпросния фактор, е най-вероятно да се превърнат в апикални клетки.
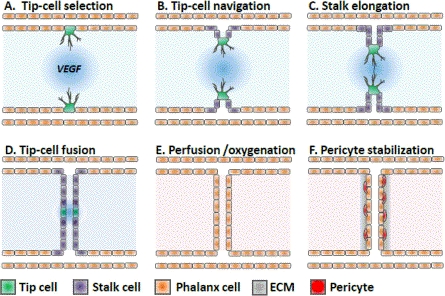
След първоначалното формиране на капилярния ствол, което е показано на горната схема за пореден път, започва така нареченият процес на матурация (узряване) на капиляра. Със син цвят е означена хипоксичната зона, която съдържа по-голямо количество васкуларен ендотелен растежен фактор. Стената на новообразуваните капиляри се стабилизира, синтезират се допълнителни количества колаген и като цяло структурата става по-устойчива на външни механични въздействия. Около капилярната стена се разполагат така наречените перицити - околосъдови клетки. Те се разполагат между базалната мембрана и ендотелните клетки и освен механичната стабилизираща функция имат и друга важна роля - при контракцията им следва разширяване на капилярния лумен, съответно се увеличава съдовият пермеабилитет. В капилярите навлиза повече кръв и тъканите се зачервяват и увеличават своя обем - формира се оток. Обратно, при релаксацията на перицитите съдовата стена колабира - съдовият лумен се затваря. Всичко това е особено силно изразено при мозъчните капиляри, но и при много други съдове в различните тъкани на човешкия организъм.
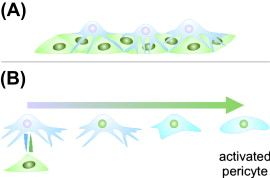
Схема на разположението на перицитите в неактивно (А) и активно (В) състояние. Контракцията им води до стабилизиране на съдовата стена, съответно до отварянето на просвета на капиляра. В много тъкани перицитите не са разположени върху базалната мембрана или такава изобщо липсва - например в черния дроб, където са налице големи синусоидални пространства. Там се откриват така наречените звездовидни клетки (клетки на Ито - името на откривателя им). Ретикуларните клетки на костния мозък също не лежат върху базална мембрана, но са тип перицити. Мезангиалните клетки в централната нервна система пък са трети тип видоизменени перицити. Подобна функция (като на перицитите) имат и периваскуларните гладомускулни клетки - те също регулират съдовия пермеабилитет, но се разполагат извън пределите на базалната мембрана. Освен това различни протеинови маркери се откриват в гладкомускулните клетки, а липсват в перицитите - което е в подкрепа на становището че двата типа клетки са коренно различни като произход и хистологичен строеж въпреки сходната си функция. В областта на главния мозък дефицитът на перицити води до увеличен пермеабилитет на капилярите - съдовата стена отслабва с всички негативни последици от това. Също така се нарушава биологичната бариера между нервната тъкан и кръвта и нервната система престава да бъде задбариерен орган. В подкрепа на това схващане са някои експерименти с животни - при деактивиране на перицитите при мишки се наблюдават микроаневризми.
При перицитите също има интензивни процеси на растеж и обратно развитие, които процеси са особено ясно изразени при заздравяването на раните. Както при ендотелните клетки, и при перицитите размножаването и апоптозата са прецизно регулирани от различни биологично активни протеини. При нарушения в регулацията започва неконтролиран растеж и се развива специфична неоплазия - хемангиоперицитом.
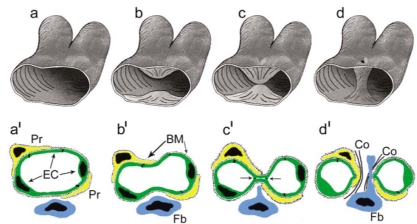
Схема на разклонителната ангиогенеза - един съд се разклонява на два ендакви по диаметър нови съда. Това е основната разлика спрямо кълновата ангиогенеза - при нея от един основен ствол се разклоняват клончета, които са с много по-малък диаметър. В една и съща анатомична област е нормално да се наблюдават и двата механизма на формиране на нови съдове.
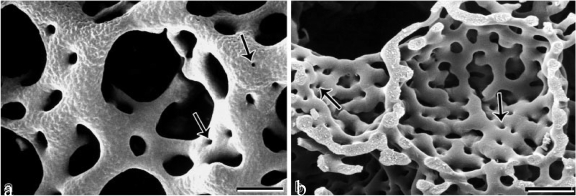
Скенираща електронна микроскопия на съдова мрежа на ембриони. Вляво, с буквата а, е показан зародишът на бял дроб на пиле. Вдясно, с буквата b, е е показан белият дроб на зародиш на плъх на възраст 44 дни. Със стрелки са означение отвори с диаметър около 2 микрометра, през които прорастват колони от съединителна тъкан.

Триизмерна схема на прорастването на нов кръвоносен съд - графичният дизайнер се е опитал да го представи като наелектризирана структура, което всъщност изглежда доста ефектно. Ендотелните клетки наистина изглеждат плоски и се подреждат под формата на маншон - което води и до формирането на нови капиляри. Клетките на тъканта, която е необходимо да се реваскуларизира, са представени с овална форма и са оцветени в сиво - синкав оттенък. Важен е въпросът за възможността за регенерация и образуване на по възможност по-големи и по-дълги нови кръвоносни съдове. Най-общият принцип в биологията е че колкото е по-висш един организъм, толкова по-малки способности за регенерация има той; обратно, нисшите организми имат изразена способност за възстановяване на органи и тъкани. Очевидно е че по-високата степен на диференциация и специализация на тъканите е за сметка на техните регенеративни възможности. Така например един гущер възстановява опашката си в рамките на няколко дни, а невроните от главния мозък на човека са изгубили способността си за деление на практика преди раждането.
При необходимост ангиогенезата може да се стимулира, което води до ускорена регенерация на тъканите - нещо, което в повечето случаи представлява полезен ефект. Богатата на тромбоцити плазма и концентрираните растежни фактори стимулират формирането на нови кръвоносни съдове, тъй като в тромбоцитите се съдържат белтъчните молекули, активиращи съдообразуването. При богатата на тромбоцити плазма този ефект е изразен добре, но при концентираните растежни фактори е още по-силен - тъй като тази субстанция съдържа разрушени тромбоцити, които са отделили всички свои съставки в активирано състояние. Стимулирането на ангиогенезата има добър ефект при периферни съдови заболявания, исхемична болест на сърцето и оздравяването на рани.
Остава открит въпросът за максимално възможният диаметър на кръвоносен съд, който може да се образува в резултат на процеса ангиогенеза.
В други случаи ангиогенезата е част от патогенетичния механизъм на тежки заболявания и е необходимо да бъде подтисната. Така например при нарастването на един злокачествен неопластичен процес формирането на нови кръвоносни съдове играе значителна роля - те изхранват тумора и помагат за неговия бурен растеж, който не зависи от регулаторните системи на организма. При подтискането на ангиогенезата съответно би могъл да бъде забавен или дори спрян и процесът на нарастване на тумора - което в съвременната онкология се използва при химиотерапията на различните неоплазии. Освен това подтискането на ангиогенезата подобрява клиничното протичане на ревматоидния артрит и някои офталомологични заболявания.
От клинична гледна точка голямо значение има въпросът за максималния диаметър на кръвоносният съд, който е способен да се формира първично или да се регенерира. От дълбока древност е известно че най-големите по размер кръвоносни съдове не могат да се възстановяват спонтанно - въпреки че много древни анатоми са смятали че по хора на артериите не тече кръв, а въздух. Въпреки множеството заблуди и погрешни представи за реалността, хората все пак са били наблюдателни и са си правели съответните изводи - при нараняване на аортата, феморалната или брахиалната артерия например е необходима оперативна намеса в свръхспешен порядък, за да се предотврати кръвозагуба в голям обем и съответно да се спаси животът на пострадалия. Всъщност сърдечният арест, задушаването от обструктивен тип и разкъсването на стената на големи артериални съдове представляват най-спешните състояния в медицината в цял свят. Те изискват реакция от страна на лекаря в рамките на 30 до 60 секунди; в случай че в близост до пострадлия няма лекар, медицинската помощ може да бъде оказана от каквито и да било присъстващи лица. Поради това в развитите държави оказването на спешна медицинска (или съответно парамедицинска) помощ се изучава във всеки курс на средното образование. При нараняване на съдове с малък калибър пък е достатъчно да се наложи компресивна превръзка, в някои случаи да се наложи шев на раната, при което тъканите се възстановяват след определен период от време. Постепенно се разработват различни техники за зашиване на разкъсани съдове, които позволяват запазването на проходимостта на съда - така се съхранява кръвоснабдяването на жизеноважни органи и тъкани.
В много случаи обаче е невъзможно да се зашие кръвоносен съд в областта на механичната травма. Това се случва понякога по чисто обективни причини - пострадалият се намира в отдалечен регион и транспортирането му до специализирано лечебно заведение ще отнеме много време, за което време патологичните промени в тъканите с нарушено кръвоснбадяване вече ще настъпят. В други случаи пък преживяемостта и виталитетът на тъканите са добри и разкриването и зашиването на увредения съд би представлявало излишна допълнителна травма. В първия случай се наблюдава частично възстановяване на анатомичната цялост и функцията на тъканите, а във втория - почти пълно възстановяване, като в лицево - челюстната област условията са почти винаги такива. Поради богатото кръвоснабдяване и множеството съдови анастомози в областта проблем с нарушено кръвоснбадяване на практика не съществува - особено при лицевите травми, но почти винаги и при възпалителните и неопластичните процеси.
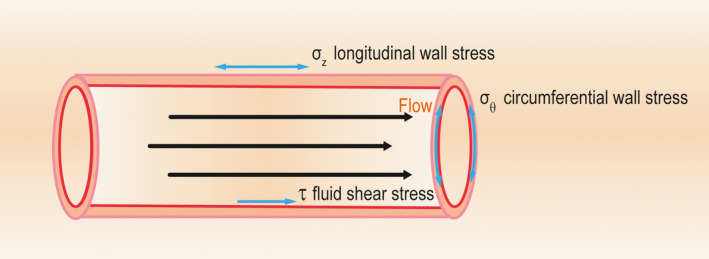
Освен ангиогенеза, през последните години в специализираните медицински издания започва усилено да се говори за така наречената артериогенеза. Това представлява един коренно различен биологичен процес, при който няма образуване на нови кръвоносни съдове - има единствено уголемяване на калибъра на артериолите, при което те всъщност се превръщат в пълноценни артерии. Чисто схематично това изглежда така:
На по-късни етапи от развитието на медицината изследователите започват да проучват ангиогенезата в различни трансплантирани органи и тъкани. Така например е установено че при автогенни костни присадки скоростта на реваскуларизация е от порядъка на един милиметър на ден - т.е. ако има присадена костна тъкан с напречен размер от 1 сантиметър, само след 10 дни тя ще бъде напълно витална, с прорастнали в нея зрели кръвоносни съдове. Това обаче е валидно само при осигурени идеални условия - пълна имобилизиция на трансплантата и пълна изолация от околната среда. Първичната стабилност е от ключово значение, както и в областта на имплантологията, за нормалното протичане на заздравителния процес. При липса на такава (например патологична подвижност на поставената костна тъкан) организмът се опитва да реваскуларизира тъканите, но при всяко движение новообразуваните капиляри, артериоли и венули се разкъсват и всичко трябва да започне отначало. Това води до влошаване и протрахирано протичане на оздравителния процес - съответно и до резорбция на трансплантата в различна степен, а понякога и напълно. При контакт на трансплантираните тъкани с околната среда и особено с устната кухина в тях навлизат микроорганизми, започва развитието на инфекция и възпаление и резултатът обикновено е катастрофален - пълна резорбция на трансплатата. Всички тези принципи са валидни с пълна сила и при трансплатнираните органи - бъбрек, черен дроб и всичко останало, тъй като и при тях ангиогенезата е от ключово значение. Допълнителен проблем представлява имуносупресията, която е наложителна при присаждане на органи от донор - тя увеличава риска от инфекция и изисква стриктна асептика и антисептика.

Първоначална ситуация - здрава костна тъкан с добре оформени кръвоносни съдове. Вижда се добре оформената кортикална пластинка - дебела кафява линия, която се разполага върху костта. Колкото е по-добро физическото развитие на организма, толкова по-силно минерализирана и плътна е кортикалната костна пластинка. При активно спортуващи или извършващи тежка физическа работа лица кортикалната пластинка се уплътнява и минерализира допълнително. От гледна точка на механичната устойчивост към травми това определено е предимство; по отношение на костната пластика обаче това е по-скоро недостатък. Прекалено плътната кост не е добре кръвоснабдена, няма перфорантни кръвоносни съдове и по принцип се характеризира със забавена обмяна. Поради това се налага преди поставянето на автогенния костен трансплантат да се проведе така нареченото декортикиране, показано на следната схема:

Отнемане на кортикалната костна пластинка - така нареченото декортикиране или декортикация. Извършва се според предпочитанята на оператора с различни хирургични инструменти - хирургична фреза (ротационен инструмент), пиезоелектричен юнит или така наречените сейф - скрейпъри. Това са остри резци (обикновено за еднократна употреба), които при няколко лентовидни движения надраскват костта, от където идва и названието им - от английски scrape - надрасквам. Хирурзи с повече въображение оприличават сейф - скрейпърите на дърводелско ренде, което е поредното доказателство че хирургията е просто един занаят, подобен на дърводелството и ковачеството. Повето инструменти от този тип имат и контейнер, който съхранява костните отпилки, при което последните могат да се поставят в друг участък от оперативното поле, където това е необходимо. В много случаи за декортикацията са достатъчни няколко перфорации на костта с малък по размер кръгъл борер. Компанията Neobiotech пък е разработила фрезата ACM - Auto Chip Maker, която служи и за декортикация, и за добив на костни отпилки - Chips, които много приличат на картофен чипс.

Дърводелско ренде - инструмент, на принципа на който работят всички хирургични сейф - скрейпъри. Самата дърводелска манипулация се нарича рендосване - отнема се повърхностен слой от дървения материал с цел детайлът да намали своя размер и да бъде напаснат там, където е необходимо. При дървеното стъбло няма толкова изразена зависимост - кората не е с по-голяма механична здравина от сърцевината, или поне в повечето случаи не е така. Различна е и идеята на манипулацията - при декортикирането на костта не се цели намаляване на размера на костта, а единствено осигуряване на достъп на подлежащите хистологични структури до оперативното поле. Крайната цел на костната пластика всъщност е увеличаване на размерите на наличната костна тъкан! Това обаче по същество не променя същността на ежедневната работа на хирурзите - те са занаятчии като всички останали и изработват краен продукт основно с ръцете си. Понякога дори се налага да използват и своя ум и креативност.
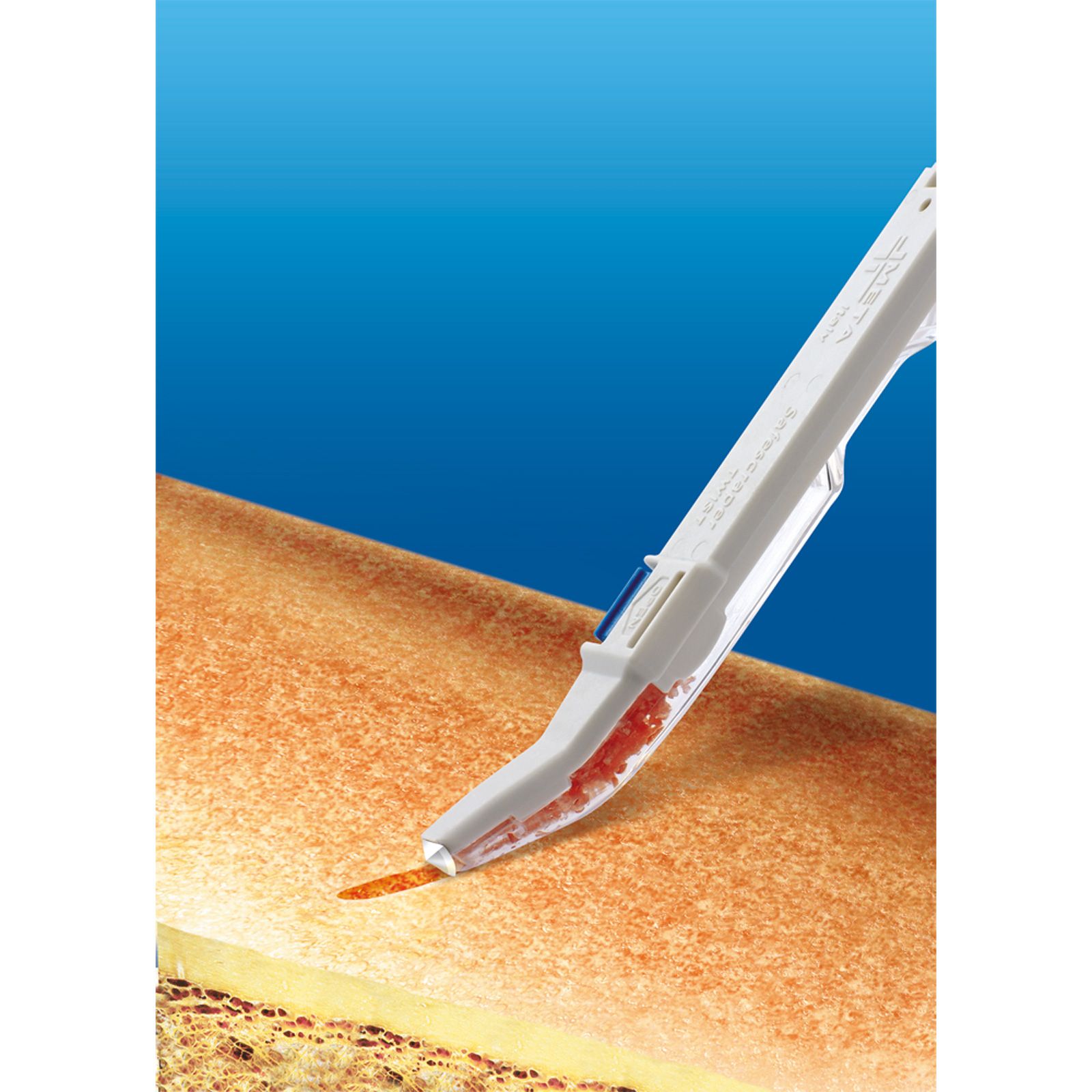
Начин на работа със сейф - скрейпъра. Достатъчно е да се надраска повърхностно кортикалната костна пластинка, за да се осигури възможност за прорастване на кръвоносните съдове от дълбоките слоеве на костта. Спонгиозната субстанция е много по-добре кръвоснабдена и е отличен източник на клетки за регенерация и дори за образуване на нова костна тъкан там, където тя не е била налична преди - което и представлява основната идея на костната пластика в имплантологията и лицево - челюстната хирургия. Нарушената цялост на кортикалната пластинка в същото време подава биохимични сигнали - в тялото е налице рана, която представлява потенциален риск за здравето, а понякога и за живота на целия организъм. Необходимо е да бъдат предприети адекватни биологични мерки за възстановяване на целостта на тъканите. Това още повече активира регенеративните процеси, включително и ангиогенезата. От дълбоките слоеве на костта мигрират клетки (остеобласти и фибробласти), кръвоносни съдове и костни морфогенетични протеини - на вътрешнофирмен жаргон нашият екип ги нарича животни, желани в оперативното поле. Други животни са изключително нежелани - например стафилококите и стрептококите.

Отваряне на контейнера и вземане на костните отпилки. Острието на сейф - скрейпъра е изключително остро и в същото време механично здраво, за да не се счупи под силата на натиска - тъй като повечето хирурзи наистина обичат да прилагат механична сила по време на ежедневната си работа. Зад острието е разположен контейнерът за костни отпилки, като повечето инструменти от този тип са еднократни. Съществуват и такива за многократна употреба, които изискват щателно механично измиване преди стерилизация. Не е допустимо въвху който и да е хирургичен инструмент да остават разпаднати белтъчни материи преди автоклавирането - въпреки че при температурите и налягането в съвременната стерилизационна апаратура микроорганизми не биха могли да оцелеят, при контакт с тъканите на следващия пациент разпаднатите и фиксирани от темепратурата материи могат да доведат до нежелани имунологични реакции. Дори и денатурирани и с нарушена структура, белтъчните молекули от замърсения инструмент представляват идеална хранителна среда за развитието на микроорганизми при вторично контаминиране - което се получава винаги в по-малка или в по-голяма степен при всяка една оперативна интервенция.
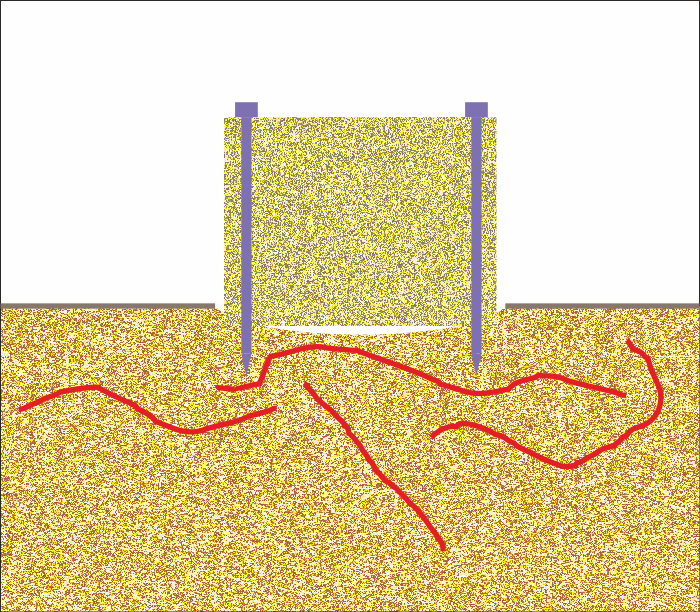
След декортикирането върху съответната област се фиксира автогенен костен блок. Фиксацията трябва да бъде трайна и механично подсигурена, за да има осигурена първична стабилност. Тук обаче е валидна с пълна сила поговорката "Прекален светец и богу не е драг". Използването на прекалено голям брой фиксиращи винтове може да има обратен ефект - да доведе до бърза костна резорбция. В костния блок се явяват зони на компресия и най-вече многото фиксиращи винтове по чисто механичен начин пречат на прорастването на новите съдове - през метал не е възможно да премине нов съд. В повечето случаи употребата на резорбируеми винтове е от полза; все пак индикациите и контраиндикациите за това следва да се прецизират, тъй като резорбируемите пластмасови винтове не осигуряват толкова добра стабилност напред във времето, отколкото титановите. Постепенно механичната здравина на връзката отслабва, винтовете се разхлабват и е възможно костният блок да се размести.
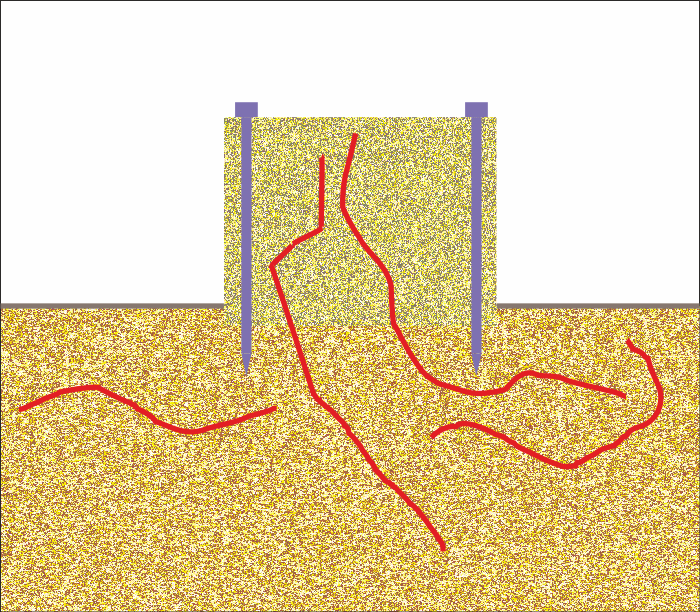
Напредък на процеса на реваскуларизация. Както вече беше споменато, скоростта на прорастване на нови капиляри е от порядъка на 1 милиметър на денонощие. Това означава че при идеални условия костен графт с линеен размер 10 милиметра ще бъде реваскуларизиран за около 10 дни, а такъв с диаметър 20 милиметра (2 сантиметра) - за 20 дни. Реалността е доста по-различна от идеалните условия и всеки практикуващ лекар е имал възможност да види това на практика. Според различни публикации в специализираната литература максималният размер на свободния костен трансплантат, който може да бъде реваскуларизиран, е от порядъка на 7 сантиметра. Над този размер спонтанните оздравителни процеси на човешкото тяло се изчерпват и е необходим различен оперативен подход - имплантиране на остеокутанно ламбо с микросъдова анастомоза - микросъдова хирургия. Според клиничните наблюдения на нашия екип дори и размер от 7 сантиметра е твърде надценен и изисква идеални условия - каквито в клиничната практика се наблюдават доста рядко. При осигуряване на микросъдова анастомоза биологичните особености на трансплантата са коренно различни - използва се вече наличната капилярна мрежа, която си е нормално анатомично образувание, при това автогенно и напълно функционално. През последните години се правят множество успешни опити за биопринтиране, но ще измине дълъг период от време преди един отпечатан на триизмерен принтер тъканен трансплантат да има биологичните особености на автогенните кожа, мускул и кост.
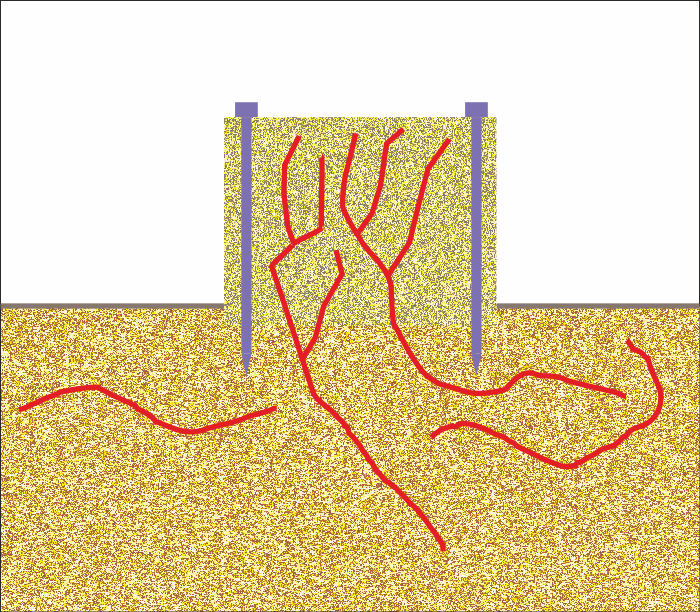
Напредък на реваскуларизацията - така нареченото узряване на трансплантата. Според много изследователи при автогенните костни присадки всъщност... няма никаква реваскуларизация. Тъй като се присажда витална кост, която е взета от собствения организъм, в нея съществува напълно функционална и анатомично изградена мрежа от кръвоносни съдове. Няма нужда от формиране на нови съдове, поради което и всъщност растеж не е необходим - и всъщност впечатляващата скорост от 1 милиметър на ден, която е доказана многократно в практиката, всъщност не е скорост на прорастване на нови съдове. Наблюдава се единствено процес на премоделиране на вече съществуващите кръвоносни съдове, както и на тяхното свързване със старите функциониращи съдове от реципиентната ложа. По своята същност обаче това не е реваскуларизация, нито ангиогенеза - това всъщност много повече прилича на артериогенезата, описана по-горе. Всички тези биологични закономерности водят до толкова бързото формиране (всъщност премоделиране) на костна тъкан и като следствие - до добрите клинични резултати при употребата на автогенни костни блокчета.
Ситуацията е коренно различна при апликацията в оперативното поле на автогенна кост с нарушена анатомична цялост - костни отпилки. За производството на подобни отпилки има конструирани голям брой хирургични инструменти - споменатите по-горе сейф - скрейпъри и различни костни мелници. Компанията Neobiotech от Южна Корея пък предлага на пазара фрезата АСМ - съкращение от Auto Chip Maker. С нейна помощ за кратко време могат да се произведат голям брой костни отпилки (чипсове), които изглеждат точно като картофени резенчета и поради това производителят е въвел именно такова название на фрезата. Предимствата на отпилките и чипсовете са безспорни - те могат да се поставят в костни дефекти с произволна форма, докато автогенният костен блок е небходимо да бъде изпиляван и моделиран. Недостатъците им обаче са значителни и много влошават клиничния резултат - при механичното раздробяване на костта всички налични кръвоносни съдове се разкъсват от мелницата и трябва да бъдат образувани от организма наново. Това твърдение е валидно с особена сила за отпилките с по-малък размер; по-големите костни фрагменти до голяма степен съхраняват своята съдова мрежа и всъщност имат повече характеристиките на монолитен костен блок. Нови кръвоносни съдове трябва да се формират единствено в зоните на свързване на отделните фрагментчета.
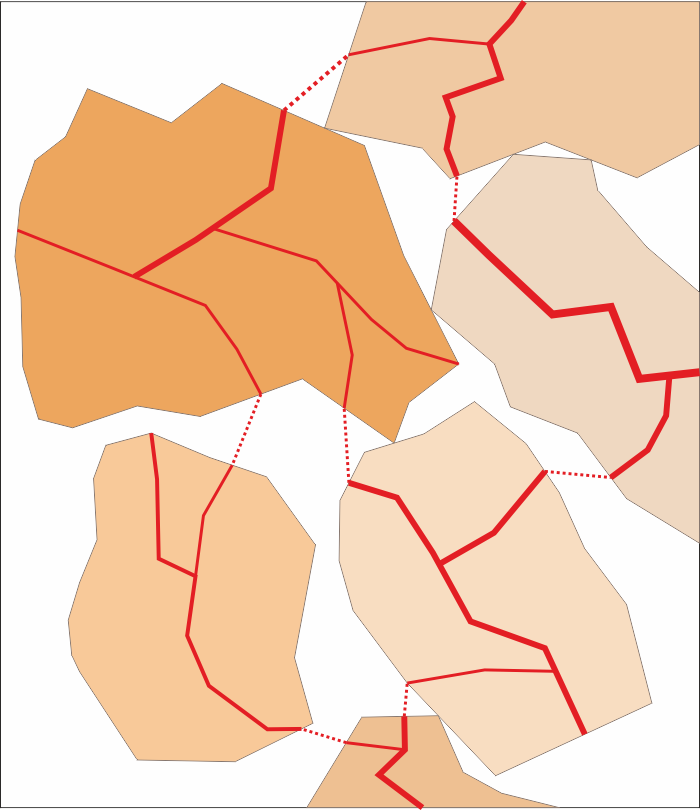
Схема на процеса на реваскуларизация при големи автогенни костни трансплантати. Те имат характеристиките много повече на монолитно костно блокче, отколкото на малки костни отпилки - които на хирургичен жаргон много често се наричат костно брашно. Едрите костни фрагменти до голяма степен имат запазена васкуларизация и, което е по-важно, между тях е необходимо да се формират минимален брой съдови мостчета - които мостчета са означени с пунктирана линия на горната графична схема. Логично е прорастването на малък на брой свързващи съдове да отнема по-малко време. В момента, в който тези връзки се образуват, всеки един фрагмент започва да се кръвоснабдява и скоро след всички заедно се свързват в плътна костна маса. Цепнатините между тези фрагменти заздравяват по механизма на заздравяване на фрактурите.
Това обаче се случва в идеалния случай. Както почти винаги се получава в медицината, реалността е доста по-различна от идеалната клинична ситуация. Проблем представлява имобилизацията на фрагментите - докато моноблокът е възможно да бъде фиксиран с винтове, едрите костни фрагменти няма как да се закрепят неподвижно към реципиентната ложа - налице е минимална подвижност. Тази подвижност обаче е достатъчна, за да се компрометира процесът на ангиогенезата. Възможно е да се извърши фиксация на фрагментите с автогенен фибрин, който се извлича от собствената кръв на пациента чрез центрофугиране - така нареченият PRF или Platelet Rich Fibrin. Този автоложен продукт освен това съдържа и голям брой растежни фактори, сред които и такива, които стимулират ангиогенезата. При големи по размер трансплантати обаче фиксацията с помощта на фибрново лепило очевидно не е достатъчно стабилна и трайна. Освен това големите фрагменти много често имат остри ръбове, които успяват да прорежат лигавицата и периоста и това води до допълнителни усложнения - пациентът се оплаква от механично дразнене, костният фрагмент бързо се инфектира от устната микрофлора и започват процеси на костна резорбция. Същите принципи са валидни и за размера на частиците на всеки един костен трансплантат - едрите фрагменти водят до доста по-чести усложнения. В някои ситуации обаче тяхната интеграция е бърза и безпроблемна а крайният резултат - доста по-добър. Това се наблюдава предимно при костни дефекти с по-голям размер, които обаче трябва да са оградени по възможност от повече страни с костни стени - големи радикуларни кисти, както и някои костни пространства на максиларния синус. Достатъчно е един костен фрагмент да се заклини (понякога дори и силово) в стените на костния дефект - тогава фрагментът придобива биологичните характеристики на костния моноблок.
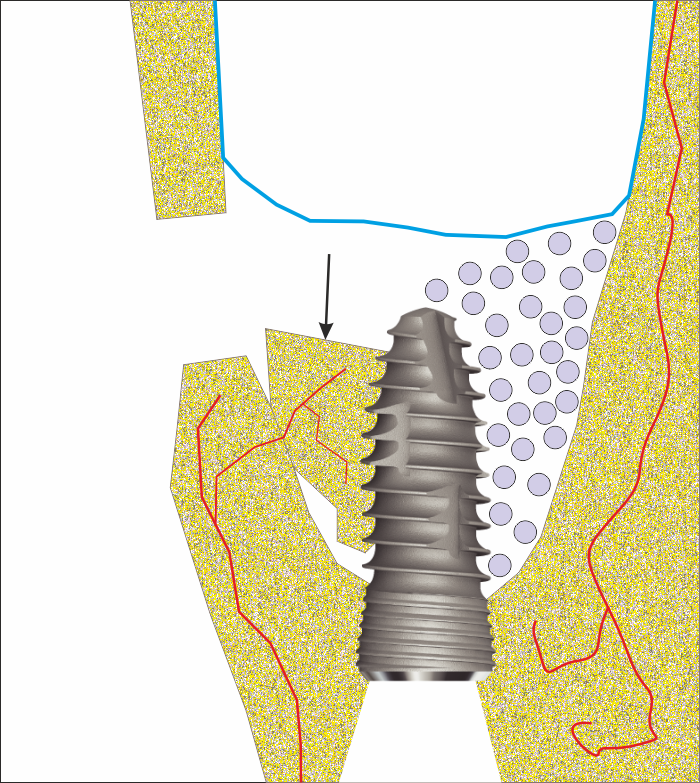
Схема на имобилизацията на автогенен костен трансплантат без винтове, единствено чрез вклиняване в костен дефект. Много често по време на оперативни интервенции в устната кухина и лицево - челюстната област се налага да се премахнат различни екзостози, алвеоларни или интердентални септи. В много случаи на същия етап се налага да се изгражда костен обем в друг участък от оперативното поле - като в този случай най-логично е да се използва собствената кост на пациента поради нейните отлични биологични характеристики. При костни дефекти с неправилна форма, какъвто е този на схемата горе, е напълно достатъчно един костен трансплантат (който най-често също е с атипична форма) да се вклини под напрежение в дефекта - това осигурява отлична имобилизация и възможност за прорастване на капиляри във фрагмента. Много често хирурзи без достатъчно клиничен опит поставят подобни трансплантати без изобщо да осъзнават колко добър лечебен подход е това; само след няколко седмици фрагментът е напълно интегриран, а полученият резултат надминава очакванията на хирурга - това представлява късметът на начинаещия.
При липса на имобилизация фрагментът започва да се резорбира и става източник на белтъчни молекули и минерални субстанции за синтеза на нова костна тъкан. Това само по себе си също представлява позитивен ефект по отношение на костната пластика, но изисква доста повече време в сравнение с имобилизирания фрагмент. Смесването на автогенната кост със синтетичен графт или ксенографт (сивите сферички) увеличава минерализацията и плътността на новообразуваната кост, при това за дълъг период напред във времето - много често и до края на живота на пациента.

При малки по размер костни фрагменти ситуацията изглежда доста по-различни - както е показано на горната схема. Те са накъсани и се реваскуларизират много по-трудно - в единица обем е необходимо да се синтезират много по-голям брой съдови мостчета между отделните костни отпилки. Точно по тази причина ситно натрошеният костен графт (дори и автогенен) има характеристиките много повече на алографт, отколкото на собствената кост на пациента. Предимствата му обаче изобщо не са за подценяване - ситно смляната кост изпълва много по-добре костния дефект и около нея не остават празнини. Малките по размер костни фрагменти не прорязват меките тъкани и не дразнят механично оперативното поле - като тази тенденция е изразена още по-силно при залепването им с автогенен фибрин, получен при центрофугиране на собствената кръв на пациента. Вероятно роля за това играе и размерът на фибриновите молекули - след полимеризацията на фибриногена те стават съизмерими с размера на частиците на графта и ги имобилизират не по-зле от остеосинтезни винтове. Вероятно и поради по-малкия си размер всеки един фрагмент, който не е фиксиран достатъчно стабилно, се подлага на костна резорбция при прорязване на периоста и не успява да проникне до устната лигавица - такива са поне клиничните наблюдения на нашия екип.
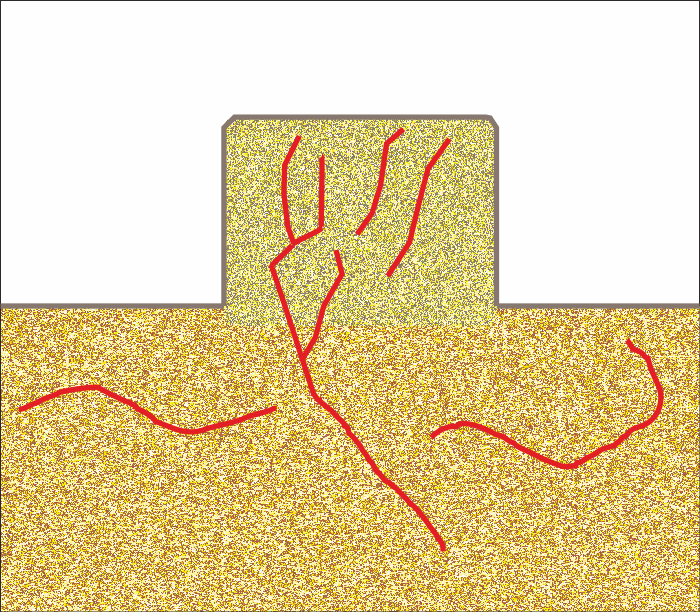
Постепенно узряването на трансплантата напредва и много скоро след пълната му реваскуларизация той на практика не се отличава от съседната здрава костна тъкан. В даден момент е необходимо да бъдат премахнати фиксиращите остеосинтезни винтове - което е показано на схемата горе. Винтовете понякога травмират надлежащите меки тъкани, а в най-лошия случай ги прорязват механично и стават причина за контакт между външната среда и костния трансплантат. При премахването им пък остават отвори, които бързо се изпълват с новосинтезирана кост; така се освобождава и пространство за поставяне на зъбен имплант, в случай че има необходимост от такъв. Много често фиксиращият винт пречи чисто механично на поставянето на импланта; в други ситуации пък оста на винта съвпада точно с протетичната позиция на импланта и това представлява голямо улеснение. В такива случаи е необходимо единствено отворът да се разшири и калиброва, след което в него се завинтва титанов имплант.
Узряването и адаптацията на един костен трансплантат е съпроводено и с известна костна резорбция на най-острите ръбове на блокчето - което е показано като заобляне на ръбовете на горната схема. Новите кръвоносни съдове достигат там в най-късните етапи на оздравителния процес, поради което тъканите се изхранват частично и започват процеси на частична тъканна атрофия - костният ръб става по-затъпен. Това обаче представлява чисто физиологичен процес, а не някакво съпътстващо усложнение. Същото се наблюдава и при оздравяването на фрактури или при нелекувани такива - при липса на лечение (или при неадекватно такова) след около 2 седмици фрактурните фрагменти заоблят своите ръбове, което донякъде затруднява адаптацията им.
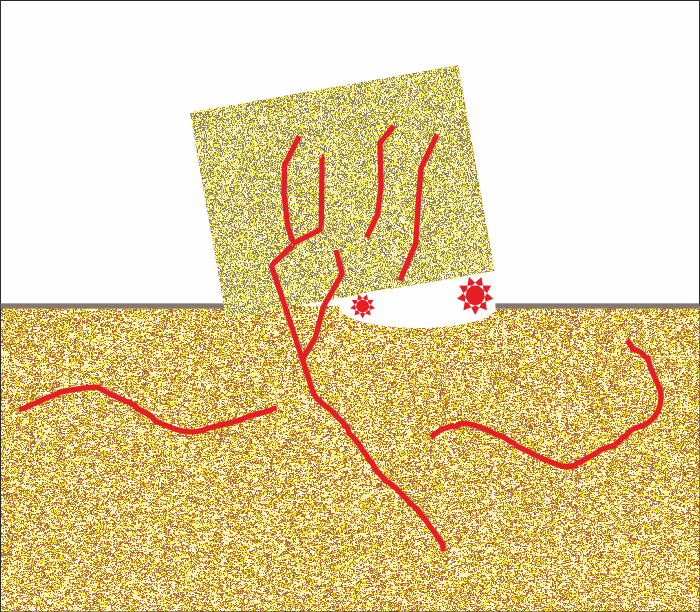
При всеки един трансплантат без микросъдова анастомоза може да възникне изключително неприятен проблем. Дори при минимална подвижност на трансплантата реваскуларизацията става на практика невъзможна. Всяко едно движение води до разкъсване на новообразуваните и прорастващи кръвоносни съдове и изхранването на автогенната кост се влошава. Това в крайна сметка води до резорбцията на трансплантата - което представлява най-честото усложнение при автогенните костни присадки. За съжаление това е и най-опасното и тежко усложнение - освен лечението на придружаващия възпалителен процес налага и поставянето на втора присадка, т.е. всичко започва отначало. Тъй като това като цяло са тежки и неприятни за пациента оперативни намеси, много често болният отказва да се подложи на последваща оперативна интервенция.
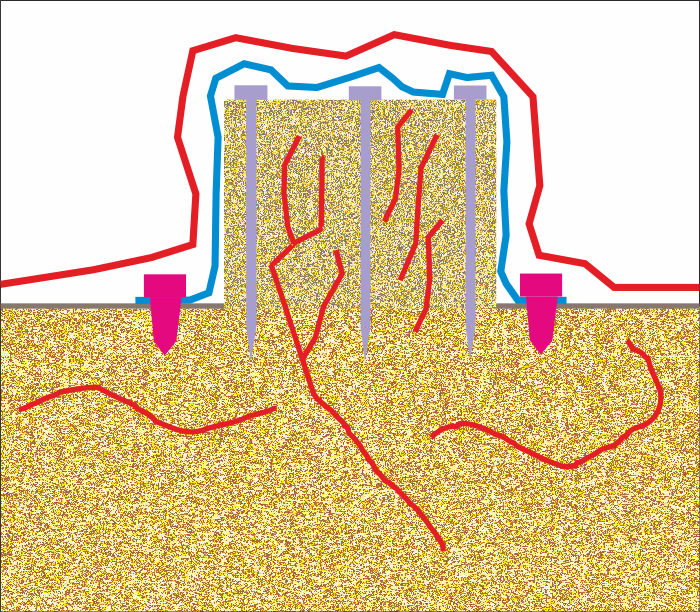
Процесите на реваскуларизация, които се наблюдават при автогенните костни присадки, протичат по аналогичен начин и при всеки един костен трансплантат от друг тип. Дори ксенографтовете и синтетичните костозаместващи материали подлежат на реваскуларизация, като това всъщност е крайната цел на всяка една аугментационна костна процедура - формирането на витална костна тъкан, която по нищо да не се отличава от нормалната кост на човешкия организъм. Проблемът при тези процедури се крие най-вече в биологичните характеристики на костозаместващите материали - при тях мрежа от кръвоносни съдове просто не съществува и е необходимо да бъде изградена от нулата. Този процес обаче е изключително бавен и изисква механична стабилност на поставеното блокче с течение на времето. Поради това на горната схема е показана фиксацията на графта с повече на брой остеосинтезни винтове - в случая три. Освен това е необходима доста по-солидна изолация на трансплантата спрямо химичните и биологичните фактори на околната среда - всякакви мембрани са полезни и силно подобряват дългосрочния резултат от лечението. Бариерната мембрана е означена като синя линия на горната графика, а винтовете, с които тя се фиксира допълнително, са оцветени в цикламенорозово. Всички тези допълнитени приспособления осигуряват оптимални условия за ангиогенезата и срастването на материала към реципиентната ложа.